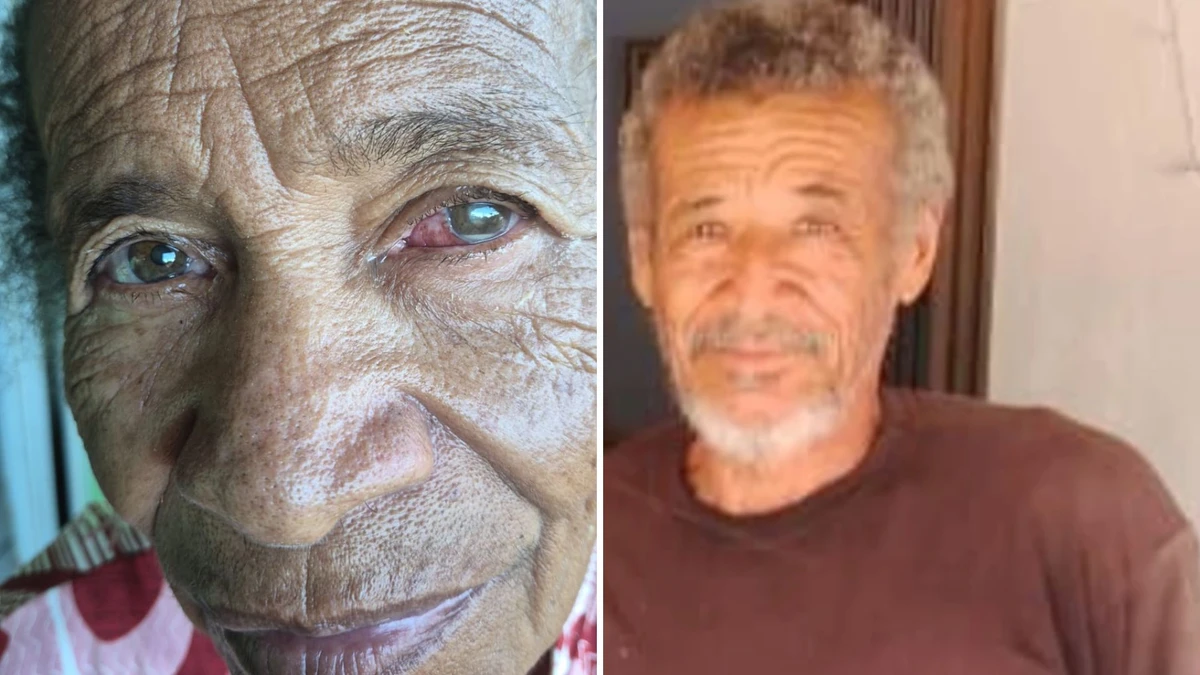
A fabricante Roche Farma Brasil informou nesta quarta-feira (8) que o medicamento utilizado no mutirão oftalmológico que deixou pacientes sem enxergar na Bahia não é indicado para os olhos. Segundo a empresa, o uso fora de bula (off-label) da substância Avastin, indicada para tratamento contra câncer, tem sido associado a eventos adversos.Como mostrou o CORREIO, mais de 20 pacientes que participaram da ação feita pelo Centro Médico e Odontológico (Hospital Ceom), em Irecê, relataram problemas de visão. Ao menos um deles precisou retirar o globo ocular. Outra idosa, de 79 anos, perdeu a visão de um dos olhos após uma grave infecção. Um paciente de 72 anos morreu um mês após o procedimento. O mutirão foi realizado entre os dias 28 de fevereiro e 1º de março. A Secretaria de Saúde do Estado da Bahia (Sesab) informou que a clínica realizou procedimentos de Terapia Antiangiogênica (TAG) em 143 pacientes, com aplicação do medicamento Avastin, agente biológico oncológico produzido pelo laboratório Roche. Ainda segundo a pasta, 26 pacientes relataram intercorrências como ardência e hiperemia ocular, dos quais 23 foram identificados como pacientes SUS.
De acordo com a fabricante, a substância tem aprovação regulatória da Anvisa desde 2002 e foi “especificamente desenvolvida, estudada e formulada para tratar vários tipos de câncer” e “não foi desenvolvida para uso oftalmológico injetável”.Em nota, o Ceom informou que “o uso de Avastin (bevacizumabe) em procedimentos de terapia antiangiogênica encontra respaldo em diretrizes clínicas e protocolos terapêuticos oficialmente estabelecidos pelo Ministério da Saúde, especialmente no âmbito do Sistema Único de Saúde (SUS), por meio dos Protocolos Clínicos e Diretrizes Terapêuticas (PCDT) aprovados pelas Portarias Conjuntas nº 18/2021 e nº 14/2021”.
Ainda segundo o centro, a prática é “amplamente consolidada na oftalmologia, utilizada no tratamento de doenças que envolvem neovascularização anômala, como a degeneração macular relacionada à idade (DMRI) e a retinopatia diabética”. “Nesse contexto, é importante destacar que o uso off-label, quando fundamentado em evidências científicas robustas, diretrizes clínicas reconhecidas e protocolos institucionais adequados, constitui prática legítima e amplamente aceita na medicina, não podendo, por si só, ser associado à ocorrência de eventos adversos”, acrescentou. Confira o posicionamento completo abaixo.